我国新冠特效药有了时间表
新冠病毒变异次数增多、变异株多国家流行,新冠肺炎疫情走势目前难以预估。在新冠疫苗取得有效防控局面的同时,对新冠病毒有效药物的需求变得越来越迫切。
那么,哪种药进展最快?究竟哪种药物的研发进展最快呢?新冠特效药目前有没有具体“时间表”?
相关资料显示,抗体药物方面,目前进展最快的是前面提到的清华大学、深圳市第三人民医院和腾盛华创联合研发的中和抗体联合疗法。
据介绍,由美国国立卫生研究院(NIH)主导该药的Ⅲ期临床试验正在美国、巴西、菲律宾等7个国家展开,研究结果乐观,BRII-196和BRII-198的联合治疗可降低78%的住院和死亡率,最有可能率先在美国等发达国家获得紧急使用授权。
在我国,研发团队已于10月9日向国家药监局滚动提交附条件上市申报材料,有望12月底前获得批准(附条件)上市。
31省区市新增本土确诊32例
11月14日0—24时,31个省(自治区、直辖市)和新疆生产建设兵团报告新增确诊病例52例。其中境外输入病例20例(上海5例,广东4例,云南4例,山东3例,福建2例,山西1例,陕西1例),含1例由无症状感染者转为确诊病例(在广东);本土病例32例(辽宁25例,均在大连市;河南3例,其中周口市2例、郑州市1例;黑龙江2例,均在黑河市;河北1例,在辛集市;云南1例,在德宏傣族景颇族自治州),含12例由无症状感染者转为确诊病例(辽宁10例,河南2例)。无新增死亡病例。新增疑似病例2例,均为境外输入病例(均在上海)。
北京11月14日零新增
1月14日0时至24时,北京无新增本土确诊病例、疑似病例和无症状感染者;新增2例境外输入无症状感染者,无新增境外输入确诊病例、疑似病例。治愈出院3例。
目前,多种由我国研发团队自主研发的新冠肺炎有效药物已经用于临床救治中。例如上面提到的筛选出两种有效中和抗体药物BRII-196和BRII-198已参与到我国700余例患者的救治当中。
在北京,一种新的中和抗体也被批准为同情用药在北京地坛医院使用。该药是由北京大学谢晓亮团队与丹序生物联合开发的中和抗体DXP604,由于有高达85%的重合位点,它使得人体细胞对于新冠病毒“拒不开门”。
在国际上,我国的新冠肺炎有效用药也在抗疫一线发挥着重要作用。资料显示,开拓药业在研的新一代雄激素受体拮抗剂“普克鲁胺”已经获得巴拉圭的紧急使用授权,其前期在巴西开展的三项临床试验初步表明,普克鲁胺能够将重症患者的死亡风险降低78%。
世界新冠疫苗研发最新进展
据中研普华产业研究院报告统计分析显示:
近期,全球多款新冠口服药物研发取得进展,给抗疫带来新希望。专家指出,疫苗和药物是互补的“组合拳”关系,未来打好抗疫“攻坚战”离不开防控措施、疫苗和治疗药物。
多款口服药获进展
本月4日,全球首款抗新冠口服药——美国默克公司和里奇巴克生物医药公司联合研发的莫那比拉韦,被英国药品与保健品管理局率先批准用于治疗特定新冠患者。据默克公司10月1日公布的Ⅲ期临床试验中期分析数据,该药可将轻中症新冠患者住院/死亡风险降低约50%,对变异新冠病毒德尔塔、伽马和缪毒株也显示出一致的疗效。
继莫那比拉韦获批后,美国辉瑞公司公布了一款疗效更优的口服抗病毒药物PAXLOVID的最新数据。Ⅱ/Ⅲ期临床试验中期分析结果显示,口服该药能降低89%的住院和死亡风险。该药由小分子药物PF-07321332和利托那韦组成,前者是针对新冠病毒主蛋白酶的抑制剂,利托那韦则是抗病毒药增效剂,此前曾用于抗艾滋病病毒。
新冠疫苗2022年上市
美国辉瑞公司公布第三季度报告公布,新冠疫苗2021年会带来360亿美元的收入。2022年COVID-19疫苗的合同额已达290亿美元,估计最后将超过2021年的销售额。
辉瑞实际上掌握着比其他人更详细而真实的疫情和疫苗数据,也做出了比美国FDA更有预见性的决策。那么,辉瑞公司对于其COVID-19疫苗的规划是如何?
辉瑞COVID-19疫苗的供应将转向欧美国家的加强针和儿童接种、低收入国家的初次接种;其已经签订的合同仍显示了非常广泛的市场需求。
这将有助于促进全球疫情的改善。 因为目前75%的疫苗应用于高收入和中高收入国家,低收入国家只使用了0.6%的疫苗。
未来行业市场投资机会在哪?欲了解更多关于行业具体详情可以点击查看中研普华产业研究院的报告《2021-2026年中国新冠疫苗行业市场行情监测及投资价值评估报告》。

 猜你喜欢
猜你喜欢 海口美兰机场专场招聘会爆棚
海口美兰机场专场招聘会爆棚  货物品种丰富多样 合肥中欧
货物品种丰富多样 合肥中欧  按下专利保护“快进键” 多
按下专利保护“快进键” 多  个人养老金制度加速崛起 金
个人养老金制度加速崛起 金  新增用户不达标、流媒体失速
新增用户不达标、流媒体失速  银行理财净值化转型进度存分
银行理财净值化转型进度存分 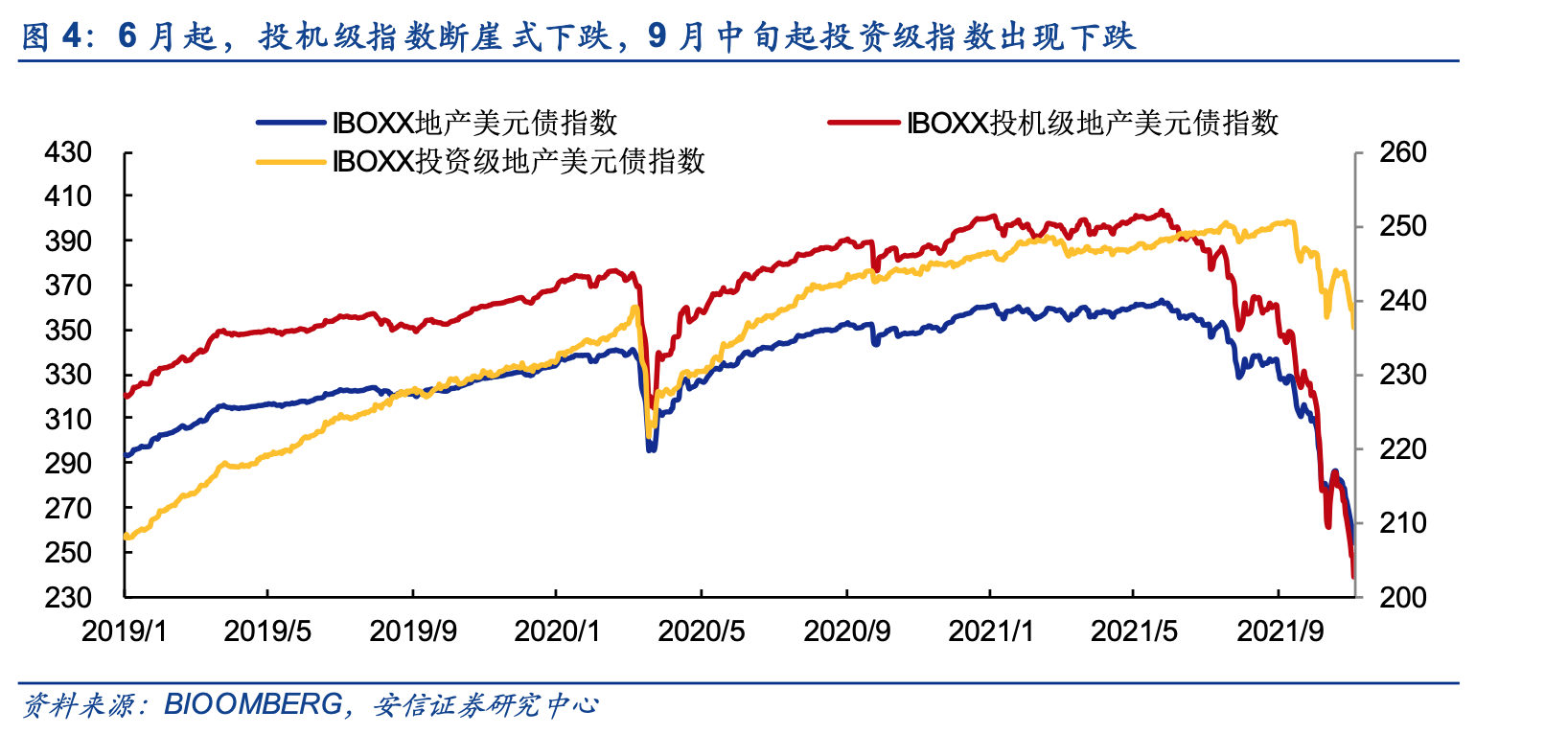 研究|地产美元债承压,债务
研究|地产美元债承压,债务  从千人嫌到万人捧 美国造车
从千人嫌到万人捧 美国造车